Tanto atteso e ora visto con sospetto. È il paradosso del vaccino contro Covid-19. Sono in molti a farsi la stessa domanda: ci sarà da fidarsi se è stato realizzato a tempo di record? Di certo, nel campo della ricerca medica, rapidità non è sinonimo di approssimazione. Il termine chiave è rolling review, revisione continua, uno strumento utilizzato dagli enti regolatori durante le emergenze sanitarie, rendere più agili i processi di verifica per accelerare l’approvazione del nuovo farmaco.
Stadi e criteri di valutazione non vengono saltati o modificati. Cambia la velocità con cui si acquisiscono i dati. In una procedura standard vengono forniti nel momento in cui si richiede l’autorizzazione per mettere un farmaco in commercio. Durante la pandemia di Covid-19, invece, i dossier sono stati revisionati in continuazione dal Comitato dell’Agenzia europea per i medicinali, che ha esaminato i risultati preliminari non clinici e le prime sperimentazioni sugli esseri umani. È successo con i gruppi AstraZeneca, Pfizer e Moderna. Dal 2 dicembre si è aggiunto il vaccino di Janssen-Cilag, azienda del gruppo Johnson & Johnson.
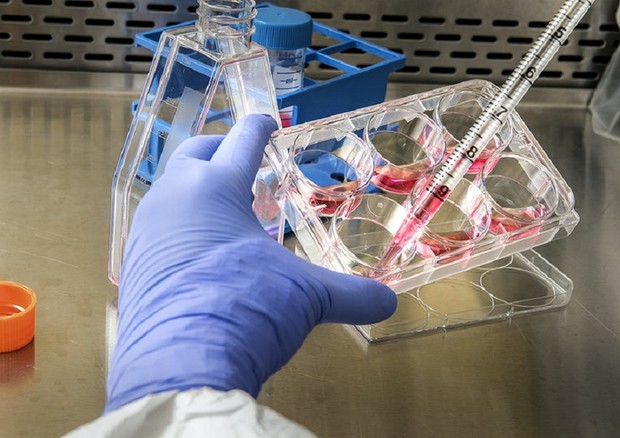
Lo stesso giorno la Gran Bretagna ha annunciato che dalla prossima settimana sarà il primo Paese al mondo a iniziare la vaccinazione contro Covid-19. L’autorità di regolazione e controllo del Regno Unito (Mhra) ha approvato il vaccino dell’azienda farmaceutica statunitense Pfizer, realizzato in collaborazione con l’industria tedesca BioNTech. «Una notizia fantastica», ha twittato il Premier Boris Johnson. Quaranta milioni le dosi acquistate, destinate a venti milioni di persone, in virtù delle due somministrazioni previste. Le prime 800.000 arriveranno entro pochi giorni. Precedenza a case di riposo per anziani, operatori sociosanitari e ultraottantenni. Nel giro di qualche mese sarà il turno di persone a rischio e over 50. Per governo e comitato scientifico, gli effetti del vaccino sulla maggioranza della popolazione potrebbero riscontrarsi da Pasqua in poi.
Ma l’Agenzia europea del farmaco (Ema) ha criticato l’iniziativa, dichiarando che il suo metodo di approvazione resta il più sicuro, efficace e basato su un maggior numero di prove. Pochi giorni fa ha ricevuto la richiesta di autorizzazione da parte di Pfizer e Moderna. Se la risposta fosse positiva, verrebbe avviata una distribuzione con procedura d’emergenza. Per il primo candidato la valutazione si terrà il prossimo 29 dicembre, il secondo sarà esaminato il 12 gennaio 2021. «Non sono i singoli Stati a trattare con le case farmaceutiche, ma la Commissione», ha affermato il ministro della Salute Roberto Speranza, durante l’informativa al Senato del 2 dicembre 2020, aggiungendo che l’Italia ha sottoscritto il 13,46% di tutti i contratti formalizzati dall’Unione e prenotato 202 milioni di dosi, tra Johnson & Johnson, AstraZeneca, Sanofi, Pfizer/BioNTech, CureVac e Moderna. Tra i punti emersi nel corso del suo intervento, la centralizzazione, la gratuità e la non obbligatorietà del vaccino. Nel nostro Paese la campagna di vaccinazione dovrebbe partire a fine gennaio 2021, diventare di massa nel primo trimestre e concludersi nel quarto. I primi a essere coinvolti saranno operatori sociosanitari, residenti e dipendenti dei presidi residenziali per anziani, e le persone con più di 80 anni. Con l’aumento delle dosi a disposizione, sarà il turno dei servizi essenziali, tra cui il personale scolastico e le forze dell’ordine.

Negli Stati Uniti, invece, la Food and Drug Administration (FDA), il corrispettivo statunitense dell’Ema, si riunirà il 17 dicembre per valutare il prodotto di Moderna. Al New York Times Anthony Fauci, direttore del National Institute of Allergy and Infectious Diseases, aveva espresso soddisfazione per i risultati ottenuti dall’azienda americana, definendoli «impressionanti». Ma in un’intervista alla Nbc il capo della task-force anti-Covid si era detto preoccupato per il ritardo nella transizione dall’amministrazione Trump a quella di Biden, perché avrebbe potuto rallentare l’approvazione e la distribuzione del vaccino.
Sono sei le società con cui l’esecutivo Ue ha stipulato contratti. I loro candidati hanno caratteristiche diverse, dalle tecnologie usate al costo sul mercato. Al momento tre sembrano in vantaggio.
Quello di Pfizer-BioNTech ha mostrato un’efficacia del 95% ed è basato sull’mRNA (RNA messaggero). Attraverso tecniche di ingegneria genetica, nei pazienti vengono iniettate nanoparticelle di grasso (grandi un miliardesimo di metro) con dentro una specifica porzione del genoma virale sintetizzata in laboratorio. Questa contiene informazioni sulla proteina Spike, prodotta grazie al “macchinario replicativo” delle cellule umane. Viene così simulato nell’individuo il primo contatto con Sars-CoV-2, evocando una risposta simile a quella dell’infezione naturale, senza però arrivare alla malattia e alle sue conseguenze. Così stimolato, il sistema immunitario si attiverà in caso di una nuova esposizione al virus.
Usa lo stesso principio il vaccino messo a punto da Moderna, azienda con sede a Cambridge, nel Massachusetts, che lo scorso 16 novembre ha rilasciato un comunicato ufficiale sui risultati della fase 3 di sperimentazione clinica: efficacia pari al 94,1%, che arriva al 100% nei casi severi. Le differenze tra i due sono nella temperatura di conservazione, dovuta all’instabilità della molecola di RNA: il candidato Pfizer necessita di -75°C, l’altro, invece, può essere stoccato a -20° e restare stabile per 30 giorni tra 2° e 8°C. Un problema organizzativo da non sottovalutare. Tra i vantaggi di questa tipologia, la produzione veloce, la possibilità di essere replicato in altri laboratori e un impiego verso vari bersagli del virus.
Non sono al momento stabiliti incontri dell’Ema per discutere il vaccino di AstraZeneca. Questo si basa su un vettore, un microrganismo che veicola l’acido nucleico del coronavirus per innescare la risposta immunitaria. Si tratta della versione attenuata dell’adenovirus dello scimpanzé, l’agente del raffreddore comune nelle scimmie, modificato in laboratorio e reso innocuo nei confronti dell’uomo. All’interno è stata inserita una porzione del genoma di SARS-CoV-2, che codifica per la proteina di superficie Spike. Costa meno dei candidati di Moderna e Pfizer, ma ha bisogno di processi produttivi più lunghi. Altro svantaggio, il sistema immunitario potrebbe non reagire alla componente vettoriale, perché troppo “familiare”.
Il percorso di questo vaccino, nato dalla collaborazione tra lo Jenner Institute dell’Università di Oxford e la società Irbm di Pomezia, è stato altalenante rispetto agli altri. Lo scorso 9 settembre la sperimentazione era stata sospesa per valutare il nesso causale tra somministrazione del farmaco e riscontro in un paziente di mielite trasversa acuta, un’infiammazione che coinvolge il midollo spinale nella sua ampiezza e blocca la trasmissione degli impulsi nervosi. Esclusa la correlazione, il trial era ripreso quattro giorni più tardi, per poi subire un’ulteriore frenata alla fine di novembre, dopo che era stato annunciato il buon esito della fase 3. Motivo? I risultati sarebbero stati raggiunti con un dosaggio diverso da quello dichiarato. Nello specifico, in circa 2300 pazienti la prima delle due dosi previste era dimezzata. In questo gruppo l’efficacia era risultata del 90%, rispetto al 60% degli altri 8900 volontari che avevano assunto la posologia completa. Così, entro una settimana, AstraZeneca spedirà la nuova documentazione per l’approvazione del vaccino agli enti regolatori.
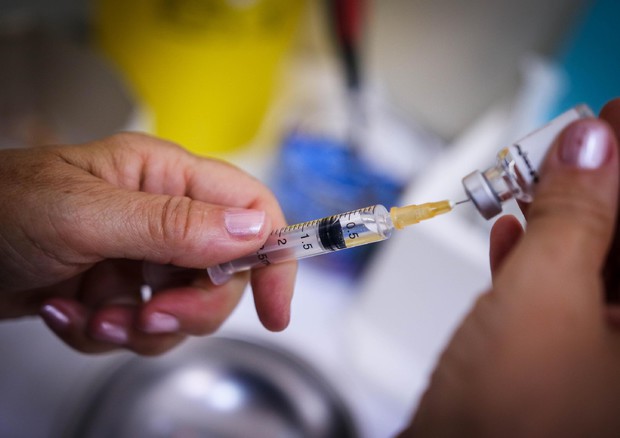
Qualunque sia il candidato che anticiperà i rivali nella volata finale, il Direttore Scientifico dell’Istituto INMI Spallanzani Giuseppe Ippolito non ha dubbi. Intervenendo il 2 dicembre a Rai News 24 ha dichiarato: «Al momento non esistono farmaci antivirali efficaci. Il vaccino è l’unica arma a disposizione».